先进生物制造正成为推动医药、食品、能源、材料等领域转型升级的重要技术路径,而高性能微生物底盘的构建,是实现其规模化与低碳化生产的关键。巴斯德毕赤酵母因其独特的代谢特性与工程潜力,正在从传统重组蛋白表达宿主走向新一代细胞工厂核心平台。
近日,我校生物工程学院蔡孟浩教授团队在生物技术权威综述期刊Biotechnology Advances(IF 12.5)发表题为“The industrial yeast Komagataella phaffii blooms for advanced biomanufacturing”的论文,系统总结了该菌株在先进生物制造中的发展路径与关键技术进展。
该综述指出,巴斯德毕赤酵母已突破单一表达宿主的功能边界,逐步形成覆盖大宗蛋白制造、天然产物合成、低碳底物转化及遗传精准调控的多功能工业底盘菌株。围绕其性能提升与功能拓展,作者从底盘演进、产物谱扩展、碳源重构及工具体系建设等方面进行了系统论述,呈现出“蛋白表达系统”向“多能细胞工厂”演进的清晰路径。
该菌株最初依托甲醇代谢及甲醇诱导型AOX1强启动子体系建立了经典蛋白表达系统。随着基因组学、系统生物学及基因编辑等技术的发展,其底盘属性被进一步激活。作为兼具高密度发酵能力与真核蛋白加工优势的宿主,该酵母在分泌表达效率、蛋白质量控制及下游纯化适配性方面逐步形成体系化优势,为其从表达系统向通用工业底盘的转型奠定了基础。
基于此,该菌株在重组蛋白制造领域持续拓展,应用范围已覆盖生物医药、工业酶、食品蛋白、饲料蛋白及生物材料等多个方向。通过对表达调控与分泌路径的持续优化,其在多类型蛋白的高效表达中表现出良好的稳定性与规模化潜力,逐步由高附加值蛋白生产平台向通用蛋白制造体系演进。
随着代谢工程与多酶协同策略的发展,该菌株在复杂天然产物生物合成方面发展迅速,已展现支持黄酮、生物碱、萜类及聚酮等多类活性分子的从头生物合成,体现稳定承载复杂代谢路径与多酶系统的能力,标志着其功能由“蛋白质合成”向“复杂化合物合成”的延伸。
区别于传统依赖糖类底物的发酵体系,该菌株在非粮碳源利用方面具有独特优势。围绕甲醇、甲酸、乙醇及乙酸等C1/C2底物的代谢重构,该酵母正逐步建立面向低碳生物制造的底物利用体系,为缓解粮食资源竞争及降低碳排放提供新的技术路径。
与此同时,遗传操作工具体系的完善正在加速该菌株的工程化进程。CRISPR/Cas9编辑系统、多位点整合、启动子与转录调控工程等技术的发展,使其逐步具备精确调控与模块化设计能力。结合多组学分析与计算设计方法,该底盘正向可预测、可编程的细胞工厂体系快速演进。
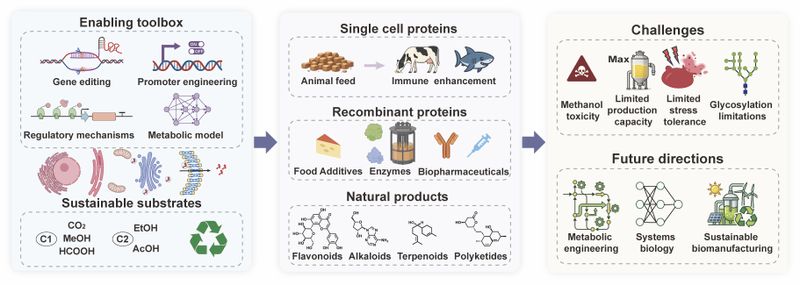
图片说明:毕赤酵母赋能先进生物制造的工程策略与应用体系
尽管巴斯德毕赤酵母已展现出广泛应用潜力,其在超高水平蛋白表达、复杂产物合成效率以及工业放大稳定性等方面仍面临挑战。未来有望通过多组学解析、动态调控、代谢工程、过程强化与代谢模型等策略,进一步提升其工程鲁棒性与产业适配能力,推动其成为通用型的生物制造核心底盘宿主。
该综述论文由我校生物反应器工程全国重点实验室蔡孟浩教授课题组完成,我校博士生吕玟、李赟浩、王世杰为论文共同第一作者,蔡孟浩教授为通讯作者。该工作得到上海市探索者计划和上海市农业科技创新项目的资助。
近年来,蔡孟浩课题组聚焦毕赤酵母甲醇诱导/碳源阻遏调控机制及重构设计,持续拓展开发多样化新型高效表达系统及配套工艺体系,适配不同工业应用场景的现实需求,相关技术已形成系列专利并实现多项转让/许可。最新研究针对其传统甲醇诱导表达系统生产应用中的易燃易爆、高耗氧、高产热等痛点,开发了葡萄糖浓度切换型诱导表达系统,实现甲醇完全解耦,使上市纳米抗体药物Caplacizumab产量达到26.6 g/L,达到已报道的纳米抗体表达最高水平(Chem Eng J, 2026, 537: 176512)。
论文链接:DOI: 10.1016/j.biotechadv.2026.108905






