近日,我校化学与分子工程学院费林加诺贝尔奖科学家联合研究中心朱为宏院士、郭志前教授团队在《美国化学会志》发表封面文章“Excitation-matchable shortwave infrared quinoliniumfluorophores:decoding spatiotemporal interactions with multiplexed bioimaging”,创新发展了基于喹啉鎓盐的短波红外荧光染料库,首次实现了激发匹配的多光谱生物成像技术,为解析活体时空相互作用提供了全新的分子可视化工具箱。

短波红外成像(SWIR,1000nm-2000nm)因其优异的组织穿透性和低背景荧光干扰,被认为是哺乳动物活体层面多重成像的理想窗口。然而,该技术长期受限于缺乏高度可调的“分子骨架核心”,现有近红外染料难以同时满足高亮度、低串扰、商用激光匹配等多重需求。为解决上述难题,研究团队从分子设计源头出发,创新地引入结构可调的喹啉鎓盐作为染料“骨架核心”,通过系统的吸/供电子性取代基修饰,设计了SWIR喹啉类七甲川菁染料(QC7 1-14,图1),其吸收波长可精准调控,覆盖975至1046nm范围,为多光谱成像应用提供了丰富的染料工具箱。
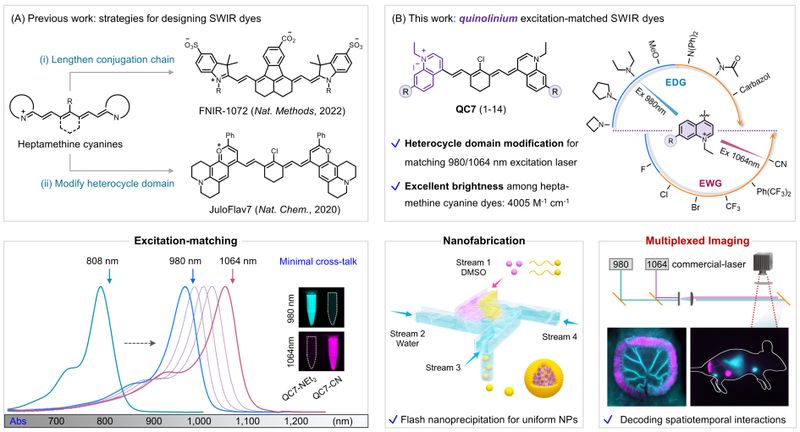
图1.近红外喹啉菁染料分子设计及活体多通道生物成像
在该系列染料中,QC7-NEt2和QC7-CN表现出超高的荧光亮度(4005M-1 cm-1),而且光谱分离性能优异,并与商用激光器波长(980nm与1064nm)高度匹配,用于多通道活体成像。基于这对“正交”染料,研究团队首次成功捕捉到了血管网络的精细结构及其动态变化、淋巴系统的实时流动、肠道蠕动的完整过程,以及多个生理系统之间的协同作用,为理解在体、复杂生理过程提供了强有力的可视化技术支撑。
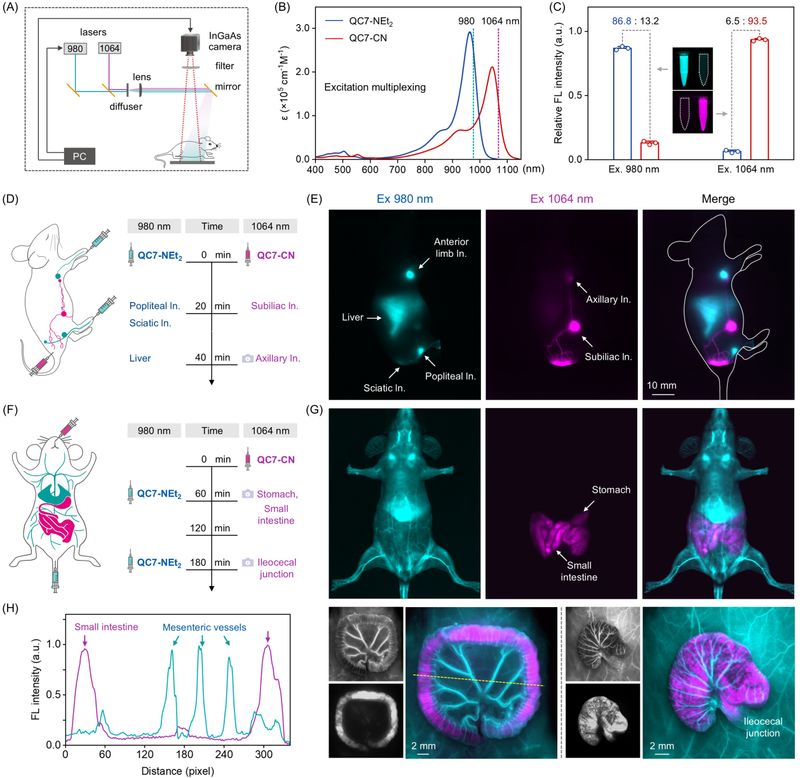
图2.QC7-NEt2与QC7-CN用于激发匹配的短波红外双通道成像
该工作主要由姚永康博士(2024届博士毕业生,现为上海交通大学附属仁济医院博士后)在燕宸旭副教授和郭志前教授的指导下完成,得到华东理工大学朱为宏院士、上海交通大学樊春海院士、仁济医院核医学科刘建军主任的大力支持。该工作得到了材料生物学与动态化学教育部前沿科学中心、费林加诺贝尔奖科学家联合研究中心、国家杰出青年科学基金、上海市“科技创新行动计划”等支持。
原文链接:https://pubs.acs.org/doi/full/10.1021/jacs.5c10749






