在生物系统中,跨膜通道的通透性可以通过化学信号的组合进行可编程调节,从而实现运输特性的刺激响应性转变,以满足不同的生理需求并适应环境变化。仿生人工纳米通道在信号调节和亚细胞生物传感方面展现出巨大潜力,然而在真实细胞的复杂环境中,实现多种化学信号的动态实时响应仍然是一项挑战。近日,我校化学与分子工程学院钱若灿副教授团队在基于化学信号门控人工纳米通道构建原位时序性响应测量界面研究取得突破性进展,相关成果以“Chemically gated artificial nanochannels for programmablesubcellular signal modulated transport regulation”为题发表于《自然-通讯》(Nature Communications, 2025, DOI:10.1038/s41467-025-66239-0)。
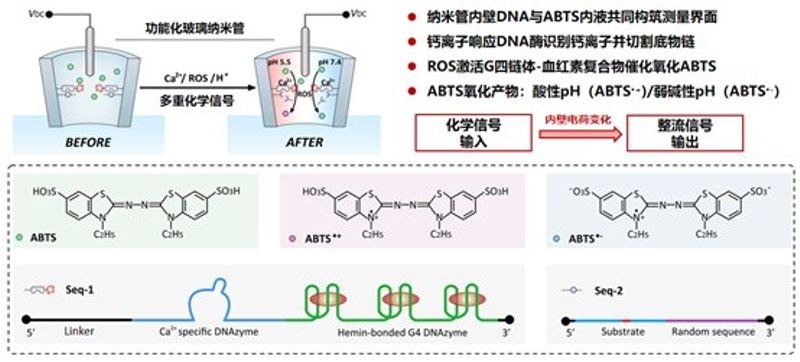
课题组研究人员设计了一种基于化学门控人工纳米通道的动态测量新策略,通过在玻璃纳米管内表面修饰DNA功能结构来实现跨膜通道的整流性质转换。DNA链的空间结构和电荷可通过多种关键化学信号进行智能调节。Seq-1包含用于纳米管内壁附着的连接部分(Linker)、钙离子响应DNA酶(CD)、G四链体-血红素复合物(HG4)三部分,Seq-2包含与Seq-1中CD部分对应的底物(Substrate)以及一段随机DNA序列(RD)两部分。CD和Substrate序列互补,Seq-1和Seq-2在纳米管内壁形成Seq-1/Seq-2二聚体(dsDNA)。用含ABTS,即2, 2’-联氮-双(3-乙基苯并噻唑啉-6-磺酸)的电解质溶液填充玻璃纳米管,建立多重化学信号响应的测量界面。Ca2+激活CD切割底物,导致Seq-2的3’端片段脱落。HG4可以催化ROS介导的ABTS氧化,在酸性pH下生成ABTS•+或在中性/弱碱性pH下氧化为ABTS•-。Ca2+触发的底物裂解以及HG4催化氧化ABTS引起纳米管内壁电荷变化,通过离子电流整流(ICR)进行实时监测。
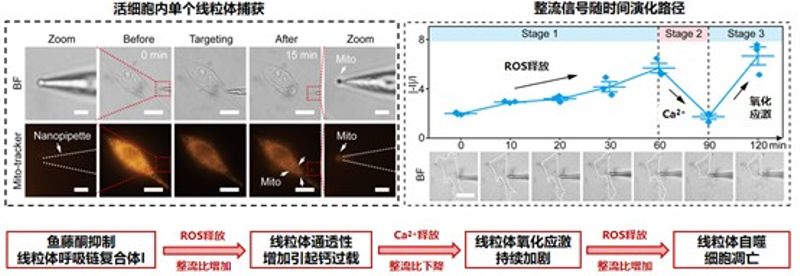
课题组实现了在单个活细胞中对单个线粒体的靶向捕获,对线粒体多种信号(Ca2+ /ROS / H+)的时序性释放进行原位响应,实现了鱼藤酮刺激下单个线粒体内源性化学信号的原位时序性响应测量。尽管细胞内环境复杂,但人工纳米通道仍能在局部亚细胞区域对复杂的化学信号进行测量。
上述研究工作由华东理工大学已毕业博士吴漫莎在钱若灿副教授指导下完成。论文第一作者为吴漫莎,通讯作者为钱若灿副教授。该工作得到了华东理工大学李大伟教授的指导和帮助,并得到了结构可控先进功能材料及其制备教育部重点实验室、费林加诺贝尔奖科学家联合研究中心的支持以及国家自然科学基金、国家科技重大专项、上海市自然科学基金等项目资助。
原文链接:https://www.nature.com/articles/s41467-025-66239-0






