近日,药学院朱维平教授课题组在新型近红外染料和纳米药物递送系统的前沿基础和应用研究中取得了重要进展,相关阶段性研究成果分别发表在BioactiveMaterials和ActaBiomaterialia。
恶性肿瘤是严重危害人类健康的一类疾病。化疗是目前治疗癌症最有效的手段之一,但是化疗药物存在毒副作用大、易产生耐药性等不足。与传统单一治疗手段相比,基于纳米材料的多模态联合治疗纳米药物递送系统具有靶向、可控释放等特点,能够提高药物稳定性和生物利用度,对增强癌症治疗效果具有重大意义。其中生物可降解纳米二氧化硅具有孔径大小可调、易于修饰、生物相容性好等特点,作为纳米载体在荧光、磁共振、光声成像以及多模态联合治疗等肿瘤诊疗领域具有较好的应用前景。
光疗法具有时空精度高、操作简单、特异性高等优点,被认为是各种肿瘤消融的新兴治疗方法。有机光治疗试剂如卟啉、酞菁、氟硼吡咯、菁染料及其衍生物等,因其具有易修饰、光物理和光化学性质可调、固有的生物降解性和良好的生物相容性等优点而受到广泛青睐。基于近红外光激发的光治疗试剂由于具有更深的组织穿透深度,可以实现更优异的光治疗效果。基于此,作者利用染料整合策略,通过模仿菁染料聚甲川链体系,设计并合成了一种新型近红外染料ML880。以商业化的新吲哚菁绿IR820作为参照,通过密度泛函理论计算发现:ML880中萘酰亚胺片段的引入可以增强电子离域,使得ML880波长发生红移。同时ML880在体外和细胞实验中表现出良好的光动力和光热效果。由于纳米装载策略可以提高染料的稳定性,肿瘤靶向性以及提供联合治疗场所,作者进一步针对肿瘤微环境中高水平活性氧,构建了一种光热/活性氧双响应的可降解药物递送系统NBD&ML@RMON,用于880nm激光和活性氧辅助的肝癌联合治疗。利用相变材料月桂酸和硬脂酸作为热响应开关,将近红外染料ML880和谷胱甘肽-S-转移酶抑制剂(NBDHEX)共同装载到可降解介孔氧化硅纳米粒子RMON中。在880nm激光照射下,ML880的光热效应可以融化相变材料,使装载的ML880和NBDHEX释放,不仅可以实现光热/光动力/化疗的联合治疗,而且可以实现治疗试剂在肿瘤区域的按需释放。该工作以题为Engineering naphthalimide-cyanine integrated near-infrared dye into ROS-responsive nanohybrids for tumor PDT/PTT/chemotherapy的研究性文章发表于Bioactive Materials。
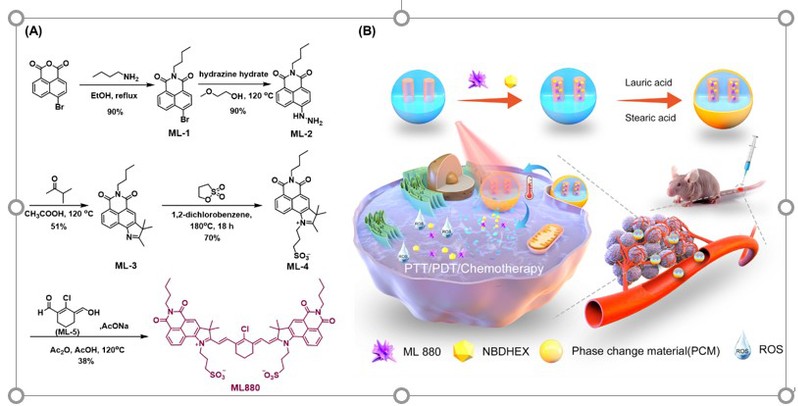
图片说明:小分子红外染料ML880的合成路线以及纳米药物递送系统NBD&ML@RMON的制备过程及作用机制
近年来,金纳米棒(GNRs)在CT/光声/光热成像方面受到研究者较多的关注,通过调节其长径比,可以制备出不同纵向等离子体共振(LPSR)吸收波长的GNRs。GNRs在与其吸收波长匹配的激光照射下具有明显的光热效应,在生物医学领域表现出良好的应用前景。由于GNRs比表面积较小,不利于药物装载及化学修饰,而介孔氧化硅具有多孔结构,可作为负载药物的载体。基于此,作者针对肿瘤细胞内高浓度谷胱甘肽(GSH),设计了可降解氧化硅包覆的金纳米棒作为药物载体,同时装载药物化疗DOX和近红外染料IR820,并在纳米颗粒表面修饰透明质酸(HA),靶向CD44受体过表达的肿瘤细胞。纳米药物IR&DOX@NC经尾静脉注射进入荷瘤鼠,通过主动靶向和被动靶向在肿瘤区域积累,并经受体介导的“内吞”方式进入细胞。在细胞内透明质酸酶和GSH作用下,HA和氧化硅壳层降解,实现药物释放。在808nm激光照射下,IR820 产生单线态氧杀灭肿瘤细胞;GNRs产生光热效应,升高肿瘤部位温度致使肿瘤细胞死亡。这种透明质酸酶/GSH双响应的纳米药物递送系统IR&DOX@NC在近红外光照下实现了肿瘤的化疗/光动力/光热联合治疗。相关工作以题为Dual-responsivenanohybrid based on degradable silica-coated gold nanorods fortriple-combination therapy for breast cancer发表于ActaBiomaterialia。
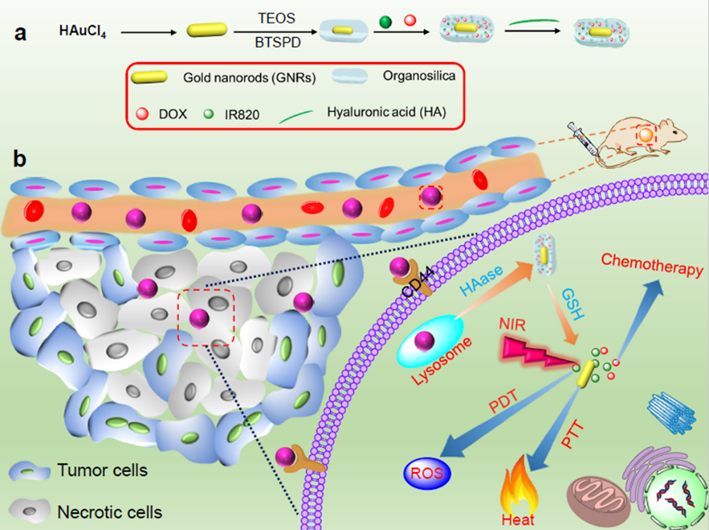
图片说明:纳米药物IR&DOX@NC的制备及其在肿瘤区域作用机制
上述工作由博士研究生金彤霞、程迪、硕士研究生计越佳等完成,得到了钱旭红院士、朱维平教授和华东师范大学孙海涛教授的悉心指导,并得到了国家自然科学基金、上海市科技重大专项等资金支持。






