6月5日,生物技术领域国际顶级权威期刊Nature Biotechnology以长文(Article)在线报道了我校生物反应器工程国家重点实验室张立新/谭高翼团队在血红素及卟啉化合物高效生物制造方向上的突破性进展。研究论文题目为“High-yield porphyrin production through metabolic engineering and biocatalysis”。这项研究标志着我校在卟啉类产品的高效生物制造方面已达到国际领先并具备产业化的水平,未来或将变革或重塑整个卟啉制造工业。

卟啉被称为生命色素,是连接无机碳到有机碳的重要节点:叶绿素(卟啉镁,负责光合作用,二氧化碳还原为碳水化合);血红素(卟啉铁,是血红蛋白生物催化的辅基,负责电子传递、运输氧)。卟啉是一种具有多种功能和活性的大环化合物,由四个吡咯环通过次甲基相连形成,具有广泛的应用。通过不同的侧链修饰和金属离子替代可以产生多种卟啉化合物,如光动力治疗中使用的原卟啉IX(PPIX)和具有抗菌活性的粪卟啉III(CPIII),以及叶绿素、钴胺素(VB12)和血红素等天然存在的化合物。这些化合物在生命活动中扮演着重要角色,并在医药、食品、饲料等领域广泛应用,其中四种卟啉化合物获得诺贝尔化学奖。此外,通过与其他过渡金属(如锰、铜、锌)螯合和侧链修饰,可以增强卟啉衍生物的光物理和电化学性能,使其在能源、诊断与治疗等领域有着广泛的应用潜力。因此,绿色、高效、低成本的生产方式对整个卟啉工业具有重要意义。传统的卟啉生产方法包括化学合成和从动物血液或植物组织中提取血红素或叶绿素,然后通过结构衍生获得其他的卟啉化合物。然而,由于结构复杂导致卟啉化合物合成较为困难,使得合成成本较高。而后者则面临着生产方式落后以及从动物血液提取可能带来的生物安全风险,在某些国家提取动物血液中的血红素是被禁止的。这些因素导致一些卟啉化合物价格昂贵,比如本研究中涉及的血红素,其国际市场上的每吨售价达到500万元-600万元,而一些卟啉中间体每毫克售价超过千元。
本研究创造性地利用光合细菌Rhodobactersphaeroides作为底盘微生物,构建高效细胞工厂,并通过偶联酶催化生产卟啉化合物的策略。首先,基于CRISPRi的关键基因筛选和调控双组分系统prrAB磷酸化水平的方法,结合分批补料发酵,在5L反应器中使目标卟啉中间体CPIII的产量达到16.5 g/L;随后设计开发了基于CRISPR/Cas12a的高通量酶筛选平台获得高效的酶催化元件,实现了CPIII的高效酶促转化,合成了各种金属卟啉,包括具有抗肿瘤活性的Zn-CPIII和具有多种功能和用途的血红素。本研究还进一步在200L反应器中实现CPIII的中试放大,并建立了基于重结晶的CPIII纯化工艺,产物纯度超过95%,回收率接近90%。在5L反应器中通过酶催化放大合成血红素和锌卟啉,产量分别达到10.8 g/L和21.3 g/L,均为迄今报道的最高生产水平。技术经济分析(Techno-economic Analysis)表明,大规模生产CPIII和血红素具有显著的成本和制造优势。这项研究提供了高效合成卟啉类产物的解决方案,为大规模生产血红素和其他具有重要工业和医学应用的有价值的卟啉提供了全新的路线,有望重塑卟啉制造工业。
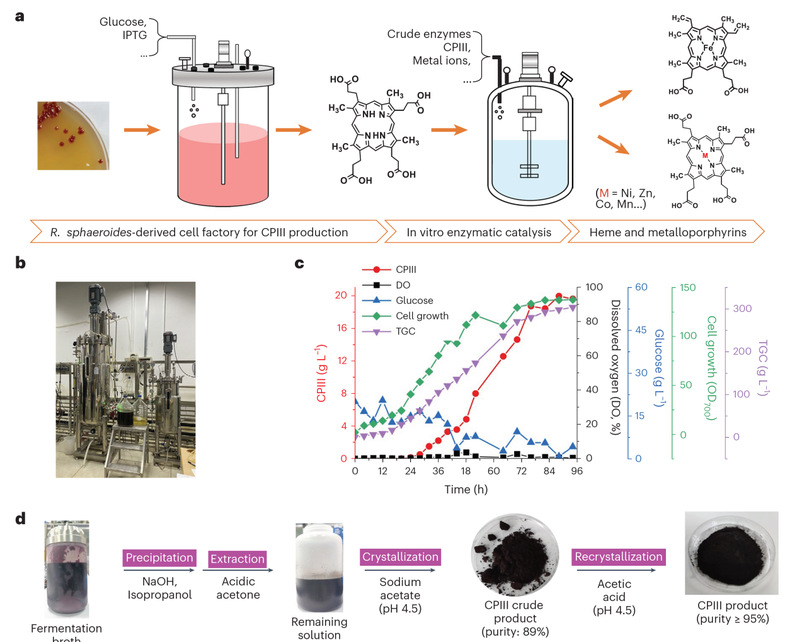
值得一提的是,酶催化在血红素合成过程中扮演着不可或缺的角色,如何获得能高效将CPIII转化为血红素的脱羧酶是本研究需要解决的关键难题。基于张立新/谭高翼团队在2019年最早提出的利用CRISPR/Cas12a和别构转录因子进行高通量检测小分子的CAT-SMELOR(猫嗅)策略(Liang, etal. Nat Commu. 2019. 10:3672),本研究利用链霉亲和素-生物素系统,将能够感应血红素的别构转录因子HrtR固定化在96孔板上,再结合CRISPR/Cas12a的高效核酸检测能力,建成了ELISA-like CAT-SMELOR(简称E-CAT-SMELOR,因操作过程类似ELISA而得名),实现了血红素的高通量检测。结合突变筛选,最终获得高活性的脱羧酶,实现了血红素的高效合成。这也是首次将CRISPR/Cas12a用于酶的高通量筛选,对酶工程具有很好的示范作用。
我校博士毕业生陈海红,硕士毕业生汪姚宏、曹婷、张璐及中国科学院微生物研究所的王为善研究员为本研究的共同第一作者。我校生物反应器工程国家重点实验室主任张立新教授和谭高翼副研究员为本研究的共同通讯作者。我校生物工程学院和生物反应器工程国家重点实验室是本研究的第一和唯一通讯单位。研究工作得到国家重点研发计划、国家自然科学基金、华东理工大学生物工程学院青年交叉创新提升计划(青椒计划)及上海交通大学微生物代谢国家重点实验室开放课题的资助。
